Учёные из университета Иллинойса взяли на себя задачу разработать антибиотик, который убивает грамотрицательные бактерии, которые часто устойчивы к антибиотикам, не уничтожая микробы, необходимые для хорошего здоровья. Если у бактерий не разовьётся устойчивость к этому препарату, это может стать значительным прорывом в лечении инфекций на долгие годы вперёд.
Профессор химии Пол Хергенротер, соруководитель исследования, сказал, что люди осознают, что жизненно важные антибиотики также имеют серьёзные побочные эффекты.
«Они убивают наши полезные бактерии при лечении инфекции, — сказал Хергенротер в пресс-релизе. — Мы хотели начать думать об антибиотиках следующего поколения, которые можно было бы разработать для уничтожения патогенных бактерий, а не полезных».
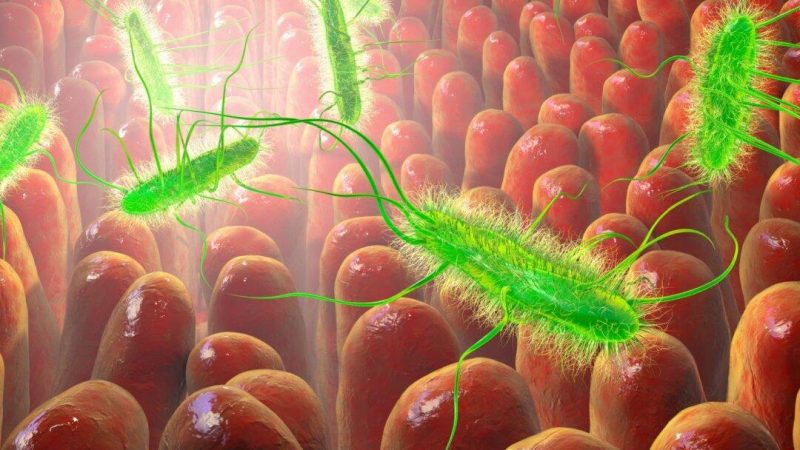
Исследование было сосредоточено на уничтожении инфекционных грамотрицательных бактерий, убить которые сложнее, поскольку они имеют двойной слой защиты. Используемые в больничных условиях препараты, уничтожающие вредные грамотрицательные бактерии, также борются с полезными бактериями, сказала Кристен Муньос, ведущий автор исследования.
«Большинство клинически одобренных антибиотиков убивают только грамположительные бактерии или убивают как грамположительные, так и грамотрицательные бактерии», — сказала Муньос в пресс-релизе.
Муньос сказала, что колистин, антибиотик, назначаемый только для борьбы с грамотрицательными бактериями, как известно, вызывает диарею, а также колит, потенциально смертельное состояние. Колистин также наносит вред печени и почкам, поэтому его «обычно используют только как антибиотик последней инстанции».
Прокладываем новый путь
Исследовательская группа заинтересовалась поиском лучшего антибиотика, потому что более 50 лет не было антибиотика, одобренного Управлением по контролю за продуктами и лекарствами США (FDA), нацеленного на грамотрицательные бактерии, которые невероятно проблематичны и трудно поддаются лечению, сказала Муньос в интервью The Epoch Times.
Практически все антибиотики, используемые в клиниках, вызывают дисбаланс в желудочно-кишечном тракте, «потому что они не делают различий между хорошими и плохими бактериями». Целью этого исследования было найти антибактериальное средство, обладающее «потенциалом селективности в отношении грамотрицательных по сравнению с грамположительными и обладающее дополнительной селективностью в отношении патогенов по сравнению с комменсалами». Симбионтные бактерии защищают иммунную систему от вторжения патогенов.
Было обнаружено, что новый препарат, лоламицин, эффективен у мышей в случаях острой пневмонии и септицемии, инфекции кровотока. По данным Центров по контролю и профилактике заболеваний, сепсис, осложнение септицемии, ежегодно становится причиной около 270 тыс. смертей из 1,7 млн случаев у взрослых в Соединённых Штатах.
«Я думаю, что самым большим выводом из этого исследования является компонент двойной селективности лоламицина, — сказала Муньос. — Здесь мы смогли разработать препарат, который воздействует не только на проблемные патогены, но и поскольку он селективен только в отношении этих патогенов, мы можем щадить полезные бактерии и сохранять целостность микробиома. Это первоначальное исследование лоламицина открывает возможности для реализации этой стратегии двойной селективности для будущей разработки антибиотиков, щадящих микробиом. Мы надеемся, что воздействие лоламицина может привести к созданию нового поколения целевых антибиотиков».
Захватывающее открытие
Муньос сказала, что на этапе тестирования многих других штаммов бактерий на мышах исследователи были взволнованы, увидев, что их гипотеза о разработке антибиотиков узкого спектра действия является многообещающей. Микробиом мышей является хорошим инструментом для моделирования инфекций человека, потому что микробиомы кишечника мышей и человека схожи. Антибиотики, которые вызывают дисбаланс микробов у мышей, оказывают аналогичное воздействие на людей.
«Было очень интересно, когда я впервые изготовила это соединение и обнаружила, что оно активно в отношении важнейших грамотрицательных патогенов, — сказала она. — Возможно, что более важно, нас больше всего интересует влияние, которое лоламицин может оказать на будущую разработку антибиотиков, щадящих микробиом».
Было также обнаружено, что лоламицин предотвращает вторичные инфекции Clostridioides difficile, серьёзную бактериальную инфекцию, обычно связанную с больницами. Было обнаружено, что он активно борется с более чем 130 штаммами бактерий в клеточных культурах, все из которых были устойчивы к множеству лекарств.
По словам Муньос, чтобы сформулировать соединение лоламицин в качестве товарного антибиотика, производителям придётся учитывать множество факторов, включая растворимость, измерение рН и оптимальную кристаллическую форму. Другие соображения будут включать дозировку и форму лекарства, такую как жидкость, таблетка или инъекция.
«Мы всё ещё немного далеки от разработки этого соединения в качестве антибиотика. Лоламицину предстоит долгий путь, прежде чем он получит одобрение FDA. К сожалению, с момента открытия антибиотика до его клинического одобрения может пройти более 20 лет. Тем временем мы продолжим изучать лоламицин. Мы хотим продолжать тестировать препарат на большем количестве штаммов бактерий и проводить более подробные токсикологические исследования».
__________
Чтобы оперативно и удобно получать все наши публикации, подпишитесь на канал Epoch Times Russia в Telegram